Desde 1930 en adelante los antibióticos han revolucionado nuestra forma de vivir. En 1928 el microbiólogo Alexader Fleming descubría la penicilina, una enzima activa proveniente del hongo de tierra Penicillum notatum, la cual era capaz de destruir las membranas de las bacterias en un proceso que Fleming denominó lisis. El descubrimiento de la penicilina se popularizó luego de la segunda guerra mundial, gracias al aporte de los productores cerveceros cuya tecnología permitió la producción masiva del antibiótico.
Luego de los descubrimientos de Fleming muchos científicos se volcaron al estudio de microorganismos ambientales en búsqueda de otros antibióticos capaces de eliminar a las bacterias patógenas. Y, vale la pena decirlo, tuvieron mucho éxito. Las enfermedades causadas por bacterias parecían cosa del pasado...
Pero la naturaleza suele tener muchas herramientas a su disposición para evitar los desbalances. Los médicos comenzaron a utilizar los antibióticos de manera descontrolada, incluso de forma preventiva. Las altas concentraciones de antibióticos en el cuerpo comenzaron a atacar a toda la flora microbiana presente en el cuerpo. Esto generó automáticamente una selección hacia los microorganismos resistentes. La resistencia a antibióticos en los microorganismos es genética y los genes que codifican para la resistencia suelen encontrarse en una estructura genética llamada "plásmido". El plásmido es una estructura circular de ADN que se encuentra dentro de la célula de la bacteria pero no está asociado a su material genético. Esto permite a las bacterias transferir este trozo de ADN a otras bacterias, y de hecho lo hacen frecuentemente. El problema es que esta transferencia horizontal de genes no es especie-específica: esto implica que una bacteria de una especie puede transferirle el plásmido a una bacteria de otra especie.
Las bacterias patógenas en algún momento comenzaron a "recibir" genes de resistencia a antibióticos. Por otra parte los antibióticos también comenzaron a utilizarse en el ganado, ya que brindan los mismos beneficios para los demás animales (además del humano). Las enormes cantidades de antibióticos generaron una respuesta desmedida en los microorganismos los cuales comenzaron a volverse cada vez más resistentes.
Un ejemplo de resistencia microbiana en ambientes con altas concentraciones de antibióticos se da en las enfermedades intrahospitalarias. Este tipo particular de enfermedades se produce por bacterias que viven dentro de los hospitales y se transmiten entre pacientes. El problema de estas bacterias es que poseen multiresistencias a antibióticos. Esto significa que poseen plásmidos que codifican para la resistencia a varios antibióticos. Ejemplos de esto son Clostridium difficile y Staphylococcus aureus MR (o MRSA por las siglas inglesas Methicillin-Resistant Staphylococcus aureus). Estos microorganismos causan enfermedades que, de no ser curadas, pueden causar la muerte del paciente. El problema radica en que, debido a que son resistentes a los antibióticos, es muy difícil curarlas.
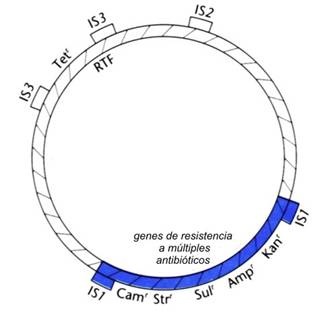 |
| Ejemplo de un plásmido con multiresistencia |
Desde el descubrimiento de la vancomicina, en 1987, no se lograron identificar nuevos antibióticos. Y, para nuestro pesar, Clostridium difficile ha conseguido volverse resistente a este antibiótico. Con esta nueva resistencia y la resistencia adquirida de otros patógenos a los antibióticos nuestras opciones comenzaron a agotarse. La posibilidad de volver a un mundo semejante a aquel previo al descubrimiento de los antibióticos se estaba convirtiendo cada vez más en una realidad.
Sin embargo, de todos los microorganismos que conocemos actualmente una gran proporción (más del 80%) son denominados "microorganismos no cultivables". Estos microorganismos tienen la característica de no crecer en nuestros medios de cultivo tradicionales. Podemos detectarlos genéticamente, pero nunca los hemos visto crecer. Y al no poder cultivarlos no podemos estudiar sus características metabólicas, entre ellas la producción de compuestos tipo antibióticos.
El grupo de investigadores liderado por Kim Lewis ha diseñado una estrategia para poder "observar" el metabolismo de los microorganismos no cultivables. Han logrado esto a través de diseñar un aparato denominado iChip que permite aislar células de microorganismos en el medio ambiente. Por lo tanto no es necesario aislar y recultivar al microorganismo, sino que simplemente sigue su vida normal en el ambiente, pero puede ser estudiado. Así, este grupo de investigadores logró detectar un compuesto producido por la bacteria Eleftheria terrae capaz de matar a bacterias multirresistentes sin generar nuevas resistencias. Este nuevo antibiótico, denominado teixobactin, está siendo probado actualmente en ratones y se cree que las primeras pruebas en humanos serán realizadas en dos años más. A pesar que el tiempo parece largo, si este antibiótico posee las mismas características que la vancomicina podemos suponer que tendremos al menos 30 años más antes que las bacterias comiencen a mostrar resistencia a este nuevo antibiótico. Aunque a largo tiempo, este descubrimiento suena prometedor y refrescante. Esperemos que así sea.
Bibliografía:
-Losee L. Ling, Tanja Schneider, Aaron J. Peoples, Amy L. Spoering, Ina Engels, Brian P. Conlon, Anna Mueller, Till F. Schäberle, Dallas E. Hughes, Slava Epstein, Michael Jones, Linos Lazarides, Victoria A. Steadman, Douglas R. Cohen, Cintia R. Felix, K. Ashley Fetterman, William P. Millett, Anthony G. Nitti, Ashley M. Zullo, Chao Chen and Kim Lewis (2015). A new antibiotic kills pathogens without detectable resistance. Nature. doi:10.1038/nature14098.
-Heidi Ledford (2015). Promising antibiotic discovered in microbial ‘dark matter’. Nature News. Publicado el 7 de Enero de 2015.
.svg/320px-Plasmid_(spanish).svg.png)
No hay comentarios:
Publicar un comentario