Entendiendo a los microorganismos en el entorno natural
Una constante en la microbiología consiste en el estudio detallado de las características fisiológicas y morfológicas de los microorganismos en cultivo puro (cabe destacar que cuando hablamos de morfología nos referimos a la micromorfología de la célula en cuanto a su forma, tipo de pared, cápside, glucocalix y otras estructuras, y a la morfología de la colonia madura para observar características como color, elevación, borde y otros). Esta detallada descripción nos da una idea de su comportamiento como individuo aislado en "condiciones de laboratorio".
 |
| Purificación de microorganismos |
 Para los microbiologos desterrar la idea de trabajar con el microorganismo en estado puro (aislado de cualquier otro microorganismo) es sumamente complicado. Desde que Robert Koch realizó sus trabajos sobre Mycobacterium tuberculosis, el agente causal de la tuberculosis, la microbiología ha estado signada por los preceptos de Koch respecto del efecto del microorganismo como agente causal de enfermedades. Y por esto hemos estudiado históricamente a los microorganismos como individuos separados del resto de sus pares.
Para los microbiologos desterrar la idea de trabajar con el microorganismo en estado puro (aislado de cualquier otro microorganismo) es sumamente complicado. Desde que Robert Koch realizó sus trabajos sobre Mycobacterium tuberculosis, el agente causal de la tuberculosis, la microbiología ha estado signada por los preceptos de Koch respecto del efecto del microorganismo como agente causal de enfermedades. Y por esto hemos estudiado históricamente a los microorganismos como individuos separados del resto de sus pares.
En los últimos años ha comenzado una nueva ola en la visión de los microorganismos. Hoy sabemos que aproximadamente 500 especies de bacterias son patógenas para el hombre. Y esto representa poco más del 5% de las especies conocidas. ¿Qué sucede con los demás microorganismos? Un atisbo de cómo viven los microorganismos en la naturaleza comenzó a vislumbrarse en los estudios de los microorganismos causantes de las caries dentales. Algo muy interesante sucedió al analizar la capa de microorganismos sobre el diente: en ella había un gran número de especies. A partir de este momento se comienza a utilizar el término "Biofilm" (la traducción sería bio-película, pero es un término tan aceptado que muchos idiomas han adoptado la palabra como propia). Al comenzar a estudiar los biofilms los microbiólogos se dieron cuenta de que este ordenamiento podría ser la clave para comprender cómo se encuentran los microorganismos en la naturaleza.
El biofilm
Los microorganismos son capaces de adherirse a una superficie y crecer sobre esta. En todo caso podemos verlo como una estrategia para una vida sésil. La movilidad en un medio acuoso puede ser ventajosa si no implica recorrer grandes distancias. Pero para un microorganismo una gran distancia podrían ser centímetros apenas (recordemos que una bacteria puede medir alrededor de 5 micrómetros o 0,0005 centímetros). Al adherirse a una superficie el microorganismo pasa a depender del medio para que lo provea. Esto no necesariamente es una ventaja; el microorganismo quedará expuesto a las condiciones del entorno. Por esta razón el microorganismo buscará protegerse. Una característica común para muchos microorganismos (bacterias arqueas y eucariotas) es la capacidad de las células de excretar compuestos complejos conocidos como EPS (por las siglas en inglés extracellular polymeric susbtaces o sustancias poliméricas extracelulares). Estas sustancias poliméricas son las que componen y estructuran el biofilm y están compuestas por una gran variedad de moléculas. El 97% del biofilm está representado por agua. Las restantes moléculas son azúcares, lípidos, proteínas ADN y algunos ácidos (entre ellos ácidos húmicos). Estas moléculas cumplen diversas funciones en el biofilm, ya sea en su estructura o en sus características.
Los azúcares son un componente mayoritario de los EPS. Los microorganismos son capaces de excretar azúcares al exterior de la célula a fin de formar un escudo que puede servir como protector contra otros microorganismos o sustancias tóxicas del medio. Los azúcares suelen estar poseer cargas negativas, lo que les permite interaccionar con compuestos catiónicos que se encuentran en el sustrato. En los procesos de bioremediación de metales se ha prestado una gran atención a esto compuestos debido a que son capaces de unirse con metales capturándolos. Se cree que los azúcares son los responsables de la adhesión al sustrato.
Los lípidos suelen estar asociados a los azúcares. Estos proveen estabilidad al complejo. De hecho, los azúcares se encuentran unidos a lípidos de membrana plasmática cuando la célula está viva. Estos azúcares se denominan comunmente glucolípidos. Es muy probable que algunos de los componentes que conforman el biofilm sean restos de células que se han lizado. Esto podría explicar la presencia de lípidos asociados a azúcares.
Las proteínas no resultan algo extraño. en su mayoría son enzimas activas que cumplen roles degradativos. Entre algunas enzimas se menciona la presencia de lipasas, proteasas y pectinasas. Sin lugar a dudas hay muchas más, pero su función en la matriz del biofilm podría no ser muy distinta a la que cumplen dentro de la célula.
El ADN extracelular (eADN) representa un misterio para los científicos. ¿Qué hace una molécula encargada de transportar información celular fuera de la célula? En un principio se sospechó que el eADN era resultado de las células lizadas, pero luego se descubrió que también cumplían función como estructurantes del biofilm (algo así como un citoesqueleto formado de hebras de ADN). Actualmente se está comenzando a sospechar que el eADN tiene una función de "comunicador" entre los integrantes del biofilm. La estructura del biofilm colabora de por sí en el quorum sensing (básicamente esta es la forma en que las bacterias hablan entre si). El eADN podría funcionar de manera aún más compleja e incluso podría permitir la producción de proteínas extracelulares.
Los ácidos están más asociados a procesos metabólicos. Es lógico que si los microorganismos se están alimentando produzcan ácidos como deshechos. La razón de que estos queden atrapados en el biofilm se desconoce. Lo que sí se sabe es que estos ácidos están involucrados en la corrosión del sustrato, permitiendo una mejor adheción del biofilm y ampliando la superficie utilizable.
Cómo se ve el biofilm
 |
| Biofilm sobre rocas |
 Los microscopios convencionales nos han permitido ver de manera bastante precisa a los microorganismos. El problema es que, al momento de montar una muestra sobre un portaobjetos, destruimos parcialmente la estructura que queremos observar. Al ver un biofilm al microscopio óptico podemos diferenciar a los microorganismos que lo componen, pero no podemos observar la estructura. Además la capacidad de amplificación del microscopio se encuentra limitada a la luz. Luego de los 1000 aumentos requerimos aceites especiales que permitan recondensar la luz para poder observar. A esta altura las bacterias, a pesar de visibles, son difíciles de observar en detalle.
Los microscopios convencionales nos han permitido ver de manera bastante precisa a los microorganismos. El problema es que, al momento de montar una muestra sobre un portaobjetos, destruimos parcialmente la estructura que queremos observar. Al ver un biofilm al microscopio óptico podemos diferenciar a los microorganismos que lo componen, pero no podemos observar la estructura. Además la capacidad de amplificación del microscopio se encuentra limitada a la luz. Luego de los 1000 aumentos requerimos aceites especiales que permitan recondensar la luz para poder observar. A esta altura las bacterias, a pesar de visibles, son difíciles de observar en detalle.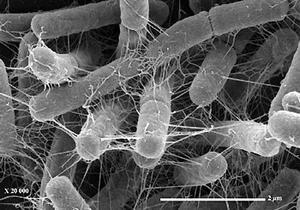 Una alternativa muy eficaz ha sido la utilización de los Microscopios Electrónicos de Barrido o SEM (por las siglas del inglés Scanning Electron Microscope). Este microscopio utiliza un concepto completamente diferente ya que bombardea a una muestra fijada con electrones de alta energía produciendo un choque de estos con los átomos de la muestra y, por consiguiente, una imagen de la dispersión de la energía. esto permite al microscopio magnificar una imagen hasta 500000 veces. Las imágenes logradas por este método son de mucha utilidad, pero poseen como desventaja el hecho de fijar y deshidratar el biofilm, lo que en última instancia hace que pierda su estructura.
Una alternativa muy eficaz ha sido la utilización de los Microscopios Electrónicos de Barrido o SEM (por las siglas del inglés Scanning Electron Microscope). Este microscopio utiliza un concepto completamente diferente ya que bombardea a una muestra fijada con electrones de alta energía produciendo un choque de estos con los átomos de la muestra y, por consiguiente, una imagen de la dispersión de la energía. esto permite al microscopio magnificar una imagen hasta 500000 veces. Las imágenes logradas por este método son de mucha utilidad, pero poseen como desventaja el hecho de fijar y deshidratar el biofilm, lo que en última instancia hace que pierda su estructura.
Actualmente se utilizan los microscopios confocales. Estos poderosos microscopios utilizan la potencia del laser para lograr generar imágenes en distintos puntos focales que no son mayores a 2 o 3 células de espesor. La sumatorioa de imágenes de una perspectiva tridimensional de la muestra tratada. A esto se lo llama comunmente Escaneo de Microscopía Laser Confocal. Además de la evidente ventaja de generar una imágen en 3 dimensiones, este microscopio permite trabajar con la muestra sin alterar. Gracias a la microscopia confocal los investigadores han logrado ver con detalle la morfología del biofilm y así entender parte de su funcionamiento.
 |
| Imagen de biofilm mediante microscopía confocal |
En la actualidad sabemos que hay una gran diversidad de formas de biofilms. Sin embargo todos comparten las características de poseer canales a través de los cuales se movilizan diversas sustancias (nutrientes, oxígeno y moléculas producidas por los microorganismos que integran el biofilm), zonas con alta concentración de agua y capas de microorganismos. Este conocimiento ha ayudado a los investigadores a dilucidar el rol de los microorganismos en el biofilm.
Cómo se estructura el biofilm
Cuando hablamos de la estructura del biofilm desde el punto de vista de la diversidad de microorganismos debemos entender que, a este nivel, estamos hablando de una comunidad. Por esta razón los microorganismos estarán organizados de tal forma que su presencia resulte en un beneficio para la comunidad en general. Actualmente se sabe que los biofilms pueden contar con una sola especie o varias (siendo esto último lo más comun). En algunos casos se ha observado una asociación de microorganismos por similitud metabólica. Un ejemplo de esto son los biofilms producidos por bacterias sulfato-reductoras. Pero también se ha descubierto que dentro del biofilm pueden producirse distintos nichos. Un ejemplo es la reducción de la concentración del oxígeno a medida que se profundiza en el biofilm. Esto permite la convivencia de microorganismos aeróbicos y anaeróbicos.
De la misma manera se producen biofilms donde intervienen microorganismos autótrofos y heterótrofos. Dado que el biofilm permite una estructura rigidizada, los microorganismos autotróficos pueden colocarse en el exterior del biofilm, quedando más expuestos a la luz solar. Las características del biofilm permiten que moléculas hidrosolubles se muevan libremente por la matriz, lo que permitiría el intercambio de nutrientes entre los integrantes del biofilm.
Y por último: ¿por qué un biofilm?
Aquí la famosa frase "la unión hace a la fuerza" jamás ha estado mejor aplicada. La estructura misma del biofilm aporta características únicas a los microorganismos que habitan en el. Los EPS son capaces de capturar moléculas cargadas eléctricamente. Se han reportado uniones tanto de cationes como de aniones a los EPS, ya que algunos de los compuestos que se pueden encontrar en esto poseen cargas positivas o negativas. Por otro lado, los EPS ejercen una fuerte selección hacia moléculas hidrofóbicas. Esto restringe aún más el ingreso de sustancias al biofilm. Los microorganismos pueden además formar capas defensivas. La muerte de las células más externas puede proteger a las más internas. Chambless y colaboradores (2006) proponen 4 mecanismos de resistencia a antibióticos por bacterias que conviven en biofilms.
Los registros de los beneficios causados por la cooperación estructural entre microorganismos en amplia. Por ejemplo, en 1988 Nakatsu y Hutchinson describieron la tolerancia a distintos metales por parte del alga Euglena mutabilis y una especie de levadura del género Cryptococcus. Estos dos microorganismos habían sido aislados en conjunto. Al convivir mostraron una mayor tolerancia a los metales en comparación a cuando eran cultivados independientemente.
De la misma manera, muchos investigadores se han volcado al estudio de los consorcios bacterianos (los cuales representan también biofilms. En este aspecto, por ejemplo Spocarti y colaboradores (2006) identificaron un consorcio de 5 especies de bacterias capaces de bioacumular metales. De la misma manera que en el trabajo de Nakatsu y Hutchinson, los investigadores compararon la tolerancia y capacidad de bioacumulación de distintos metales por parte de cada microorganismo por separado y el consorcio. Nuevamente los microorganismos asociados en consorcios mostraron ser más tolarentes a los metales y capaces de bioacumularlos en mayor cantidad.
Los biofilms no son novedosos en la naturaleza. A medida que ampliamos nuestro conocimiento sobre la microbiología ambiental nos damos cuenta que los microorganismos suelen asociarse de manera sinérgica. ¿Quién puede culparlos? Los beneficios son inegables. Es por esto que nuestros paradigmas sobre como vemos a los organismos en la naturaleza está cambiando. ¡Y ya era hora!
Los registros de los beneficios causados por la cooperación estructural entre microorganismos en amplia. Por ejemplo, en 1988 Nakatsu y Hutchinson describieron la tolerancia a distintos metales por parte del alga Euglena mutabilis y una especie de levadura del género Cryptococcus. Estos dos microorganismos habían sido aislados en conjunto. Al convivir mostraron una mayor tolerancia a los metales en comparación a cuando eran cultivados independientemente.
De la misma manera, muchos investigadores se han volcado al estudio de los consorcios bacterianos (los cuales representan también biofilms. En este aspecto, por ejemplo Spocarti y colaboradores (2006) identificaron un consorcio de 5 especies de bacterias capaces de bioacumular metales. De la misma manera que en el trabajo de Nakatsu y Hutchinson, los investigadores compararon la tolerancia y capacidad de bioacumulación de distintos metales por parte de cada microorganismo por separado y el consorcio. Nuevamente los microorganismos asociados en consorcios mostraron ser más tolarentes a los metales y capaces de bioacumularlos en mayor cantidad.
Los biofilms no son novedosos en la naturaleza. A medida que ampliamos nuestro conocimiento sobre la microbiología ambiental nos damos cuenta que los microorganismos suelen asociarse de manera sinérgica. ¿Quién puede culparlos? Los beneficios son inegables. Es por esto que nuestros paradigmas sobre como vemos a los organismos en la naturaleza está cambiando. ¡Y ya era hora!
Bibliografía
Chambless, J. D.; Hunt, S. M. & Stewart P. S. (2006) A three-dimensional computer model of four hypothetical mechanisms protecting biofilms from antimicrobials. Applied and Environmental Microbiology, 72(3):2005-2013.
Davey, M. E. & O'toole, G. A. (2000) Microbial Biofilms: from Ecology to Molecular Genetics. Microbiology and Molecular Biology Reviews, 64(4):847-867.
Flemming, H-C. & Wingender, J. (2010) The biofilm matrix. Nature reviews. Microbiology, 8(9):623-633.
Pal, A. & Paul, A. K. (2008) Microbial extracellular polymeric substances: central elements in heavy metal bioremediation. Indian Journal of Microbiology, 48(1):49-64.
Peacock, A. D.; Chang, Y-J.; Istok, J. D.; Krumholz, L. R.; Geyer, R.; Kinsall, B.; Watson, D.; Sublette, K. L. & White, D. C. (2004) Utilization of microbial biofilms as monitors of bioremediation. Microbial Ecology, 47(3):284-292.
Singh, R.; Paul, D. & Jain, R. K. (2006) Biofilms: implications in bioremediation. Trends in Microbiology, 14(9):389-397.
Sprocati, A. R.; Alisi, C.; Segre, L,; Tasso, F.; Galletti, M. & Cremisini, C. (2006) Investigating heavy metal resistance, bioaccumulation and metabolic profile of a metallophile microbial consortium native to an abandoned mine. Science of the Total Environment, 366(2-3):649-658.
van Hullebusch, E. D.; Zandvoort, M. H. & Lens, P. N. L. (2004) Metal immobilisation by biofilms: Mechanisms and analytical tools. Reviews in Environmental Science & Biotechnology, 2:9-33.



No hay comentarios:
Publicar un comentario